美国Caliper Life Sciences公司Andrea Chow博士认为,微流控技术的成功取决于技术上的跨界联合、技术和应用,这三个因素是相关的。他说:“为形成联合,我们尝试了所有可能达到一定复杂性水平的应用。从长远且严密的角度来对其进行改进,我们发现了很多无需经过复杂的集成却有较高使用价值的应用,如机械阀和微电动机械系统(MEMS)。改进的微流控技术,一般用于蛋白或基因电泳,常常可取代聚丙烯酰胺凝胶电泳。进一步开发的微流控芯片可用于酶和细胞的检测,在开发新prescription面很有用。推动微流控芯片技术的进步。定制微流控芯片材料
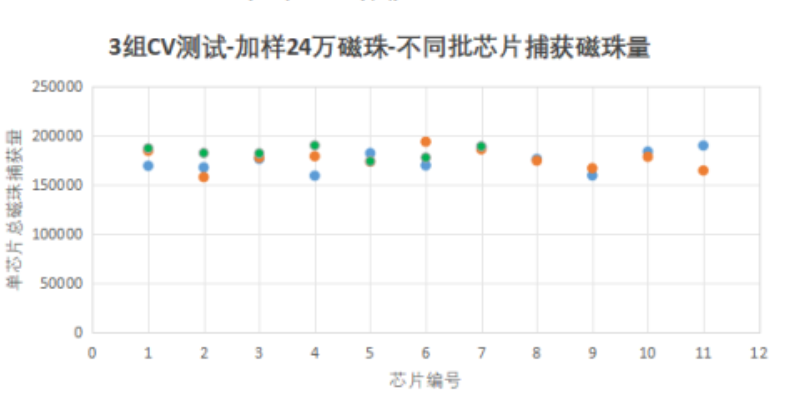
利用微流控芯片对tumour标志物检测:通过检测tumour特异性生物标志物含量可以在早期得知患病信息,也可用于监测抗tumour药物治疗效果。在tumour检测领域,Regiart等研制一种用于tumour生物标志物检测的超敏感便携式微流控设备,总检测时间只需20 min,具有稳定性高、携带方便、敏感性高等优点。由于tumour的分子机制复杂,不能依靠单一生物标志物来诊断,同时测定一组生物标志物可显著提高诊断的特异性和准确性。Jones等人设计了一款可同时检测8种标志物的微流控免疫芯片,用于诊断前列腺cancer并区分是否具有侵袭性,以减少患者不必要的活检和手术。重庆微流控芯片产业化在微流控芯片上检测所需要被检测的样本量体积往往只需要微升级别。
微流体的操控的难题:自动精确地操控液体流动是微流控免疫芯片的主要挑战之一。目前通常依赖复杂的通道、阀门、泵、混合器等,通过控制阀门的开关实现多步骤反应有序进行。尽管各种阀门的尺寸很小,但使阀门有序工作需要庞大的外部泵、连接器和控制设备,从而阻碍了芯片的集成性、便携性和自动化。为尽可能减少驱动泵等辅助设备以使系统小型化,Mauk等研究人员结合层压、柔韧的“袋”和“膜”结构来减少或消除用于流体控制的辅助仪器,通过手指按压充气囊或充液囊实现流体驱动。此外研究人员还尝试通过复杂的多层设计,更利于控制试剂加载、液体流动,如Furutani等人开发了一种6层芯片叠加黏合而成的光盘形微流控设备,每一层都有其特定功能,如加载孔、储液池、反应腔等,尽可能避免降低敏感性。
公司独特的MEMS多重转印工艺:将硅母模上的微结构通过紫外固化胶转印至硬质塑料,可在10个工作日内完成从设计到成品的全流程开发。以器官芯片为例,通过该工艺制造的PMMA多层芯片,集成血管内皮屏障与组织隔室,可模拟肺、肝等的生理功能,用于药物毒性评估时,数据一致性较传统细胞实验提升80%。此外,PDMS芯片凭借优异的气体渗透性(O₂扩散系数达3×10⁻⁵cm²/s),广泛应用于气体传感领域,其标准化产线可实现月产10,000片的高效交付。
MEMS 工艺实现超薄柔性生物电极定制,用于脑机接口电刺激与电信号记录。

肾脏组织微流控器官芯片(KoC):传统方法或常规方法的局限性,例如细胞功能和生理学的变化或不适当,使得肾单位的病理生理学研究不准确且容易出错。相比之下,与微流控技术的集成已被证明可以产生更好和更精确的结果。KoC基本上是通过将肾小管细胞与微流控芯片技术相结合来制备的。它主要用于评估肾毒性。在临床前阶段能筛查出2%的失败药物,利用微流控技术能在临床阶段后检测出约20%的失败药物。这证明了使用KoC在单个微型芯片上研究人类肾单位的合理性。微流控芯片技术用于药物筛选。中国香港微流控芯片系统
深入了解微流控芯片。定制微流控芯片材料
肠道微流控芯片(GoC):GoC系统模仿人类肠道的生理学。它解释了肠道的主要功能,即消化、营养物质的吸收、肠神经的调节、体内废物的排泄、以及伴随微生物共生体的人体肠道的病理生理学。GoC模型主要用于精确复制具有所需微流控参数的肠道体内环境。Kim等人研究了当人类GoC被肠道微生物群落占据时肠道的蠕动运动。通过对齐两个微通道(上部和下部)来设计微型器件,该微通道雕刻在PDMS层上,该PDMS是通过基于MEMS的微纳米制造工艺制作的模板翻模制备而来,且PDMS层由涂有ECM的多孔柔性膜隔开。如图所示,该装置被模仿人类肠道生理学的人肠上皮细胞包裹。这样的系统可以模拟人类肠道在某些特定因素下的蠕动运动,即流体流速。定制微流控芯片材料