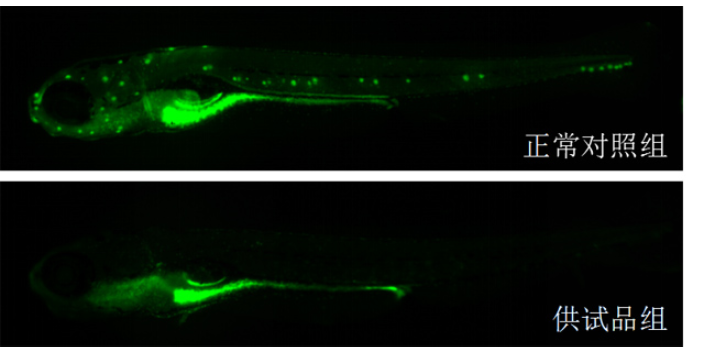
静脉注射给予长春瑞滨造模斑马鱼抵抗力低下模型。大剂量长春瑞滨骨髓抑制明显,导致血小板、红细胞及白细胞数目(中性粒细胞、巨噬细胞、T细胞等)减少和贫血,导致抵抗力低下。人类与斑马鱼在免疫系统的细胞组成上极为相似,而且斑马鱼是目前所有同时具有特异性免疫和非特异性免疫动物个体中体积较小的,适合高通量评价调节免疫功效。斑马鱼静脉注射大剂量长春瑞滨后可造成免疫低下。采用转基因T细胞红色荧光斑马鱼,可在荧光显微镜在观察到抵抗力低下的斑马鱼体内的T细胞荧光强度明显减弱药物临床前研究实验-药物功效与安全性评价。药物相互作用试验
利用斑马鱼模型评价抗气滞血瘀型血栓作用【评价原理】斑马鱼的基因与人类基因的相似度达到87%,斑马鱼血液系统与人类血液系统的血小板和凝血因子有许多共同点。大剂量肾上腺素(AH)能够引起动物血管内皮损伤和血小板活性增强,造成体内处于高凝状态。肾上腺素的大量增加模拟人体暴怒、大怒,导致气机阻滞,气滞血瘀。经过特异性红细胞染色(邻联茴香胺染色),患有血栓的斑马鱼在尾部静脉会布满红细胞,可以明显被观察到。本实验证实了阿司匹林和氯吡格雷具有明显抗血栓作用。药物安全性有效性评价斑马鱼模型评价心血管毒性。

药物开发理论上是一个有逻辑、有步骤的过程,在这一过程中,早期小规模研究的信息用于支持规模更大、目的性更强的后续研究。因此各期临床研究的目的是不尽相同的。I期临床试验I期临床试验是初步的临床药理学及人体安全性评价试验。目的:I期临床中耐受性试验目的是对新药的人体初步安全性进行评价,是评价人体对药物的耐受性、了解药物动力学及药效学分类、药物代谢和药物相互作用的研究、评估药物活性。内容:为达到以上目的,就需要进行剂量——耐受性研究(即初试剂量和耐受性评估),单剂量、多剂量的药物动力学和/或药效学研究,药物相互作用研究。
脑出血是指非外伤性脑实质内部血管破裂引发的脑内出血病症,占全部脑卒中的20%~30%,急性期病死率为30%~40%。羟甲基戊二酸单酰辅酶A还原酶(HMGCR)是他汀类药物发挥抑制作用的直接作用点,HMGCR功能被抑制会影响血管的完整性和稳定性,诱发脑出血。由于斑马鱼大脑具有典型脊椎动物脑部形态学特征,血管与神经系统在分子信号通路上与人和哺乳动物的同源性达到85%以上。在大量摄入辛伐他汀后,斑马鱼脑部也会出现脑出血的情况,患有脑出血的斑马鱼的脑部会出现明显的片状出血,而正常斑马鱼没有;由于脑出血斑马鱼的心搏输出量和血流速度也会降低,利用血流分析仪可明显观察到。脑出血可直接造成反应迟钝、运动功能障碍,可通过行为分析软件观察斑马鱼的行为轨迹。我们评价斑马鱼脑出血有4个指标:1.脑出血发生率;2.心搏输出量;3.血流速度;4.行为学(运动改善)。斑马鱼模型评价半数致死浓度。
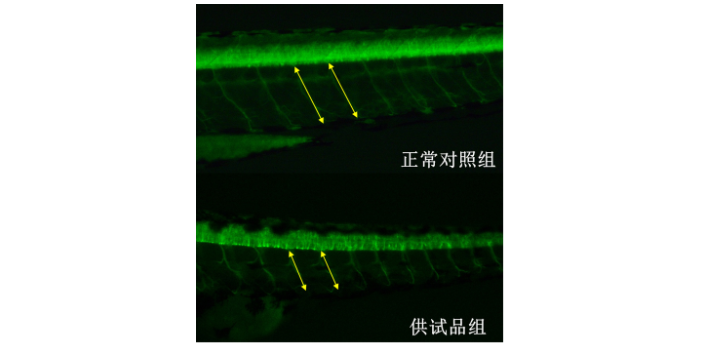
利用斑马鱼模型评价保护肾脏功效。肾脏是人体的重要组成部分,,发挥着从血液中滤过代谢废物并维持体内正常酸碱和渗透压平衡的重要作用。斑马鱼的肾脏与哺乳动物肾脏的发育及疾病的发生、发展存在很多相似之处,涉及的许多基因具有高度保守性。因此,斑马鱼适合用于评价保护肾脏功效。马兜铃酸主要损伤肾小管上皮细胞,导致肾间质纤维化及肾萎缩,并出现低分子蛋白尿、严重贫血症状,被称为“马兜铃酸肾病”。在人体和斑马鱼上,马兜铃酸均可诱发肾性水肿和肾脏形态功能异常,引起不可逆性肾损伤并至死亡。评价保护肾脏功效有两个指标:1.肾性水肿发生率。由于斑马鱼通体透明,肾性水肿可以明显的被观察到。2.肾小球滤过率。通过注射荧光物质,正常斑马鱼可将荧光物质排出体外,肾小球滤过功能损伤的斑马鱼不能将荧光物质排出体外。观察斑马鱼全身荧光强度可分析肾小球滤过率。斑马鱼模型评价急性毒***理试验价格
关于药物安全性的评价。药物相互作用试验
斑马鱼胃肠道粘膜屏障系统由较完整的机械屏障、化学屏障和免疫屏障构成,与哺乳动物高度相似,可作为胃肠道粘膜屏障研究的动物模型。三******磺酸(TNBS)可破坏肠道粘膜屏障,与肠组织蛋白结合形成抗原,发生变化反应,诱发结肠炎。杯状细胞主要分泌黏蛋白,形成黏膜屏障以保护上皮细胞,肠黏膜损伤时杯状细胞数量减少。我们可以应用特异性的染料(呈蓝色),观察肠道杯状细胞数目,评价肠道粘液分泌功能。 我们将受测试斑马鱼分成三组,分别是正常对照组、模型对照组和服用肠道粘膜辅助保护剂组。其中正常对照组未经任何处理,模型对照组与服用肠道粘膜辅助保护剂组都摄入了等量的TNBS(TNBS通过溶解到养鱼用水中的方式摄入到斑马鱼体内)。服用肠道粘膜辅助保护剂组在TNBS诱导肠道粘膜损伤之后摄入类似的肠道粘膜辅助保护剂。服用一段时间肠道粘膜辅助保护剂后,我们观察和分析肠道杯状细胞数目。药物相互作用试验