- 产地
- 苏州
- 品牌
- 外泌体提取试剂
- 型号
- 齐全
- 是否定制
- 是
外泌体的提取、分离方法:微流控技术。微流控是利用微纳米级尺寸的管道来处理和操控流体所涉及的一门技术,其在外泌体分离方面的应用受到越来越多学者的关注。Jie等[16]课题组开发了一种三维纳米结构微流控芯片,微柱阵列通过化学沉积将交叉多壁碳纳米管功能化,然后其就可以识别特定的分子(CD63)并利用独特拓扑纳米材料高效的捕获外泌体。Wunsch等[17]利用硅工艺生产纳米级确定性侧向位移(Nano-DLD)芯片,得到了均匀的间隙尺寸,该芯片可以灵敏地将20~110nm的颗粒分离。该研究证明了外泌体基于大小的位移,从而揭示了利用芯片分选和量化纳米级生物胶体的潜力。外泌体的特殊结构和功能,使得它具有潜在的应用价值,可以作为诊断多种疾病的生物指标。杭州正规外泌体提取试剂

外泌体可通过流式、WB(检测指标有CD9,CD63,CD81)、电镜观察、NTA粒径追踪等手段检测,普遍应用于药物载体、疾病诊断marker、精细医疗、一些病症治病等方面研究。由于外泌体直径小,样本含量低,提取十分困难。已有的外泌体分离方式有密度梯度离心、超滤离心法、免疫磁珠抗体捕获、商用试剂盒等。但到目前为止,仍没有一种提取方法能同时保证外泌体的含量、纯度以及生物活性。外泌体是细胞间进行物质运输和信息交流的重要工具,可以通过调节免疫功能促进一些病症的增殖,血管新生和一些病症转移。与细菌传染,帮助细菌逃避免疫关系很大,并与心血管疾病,老年痴呆等疾病具有密切关系。芜湖外泌体提取试剂供应商外泌体提取的方法:过滤。

外泌体的提取主要包括以下几种方式。一是超速离心法,这是目前外泌体提取较常用的方法。此种方法得到的外泌体量多,但是纯度不足,电镜鉴定时发现外泌体聚集成块,由于微泡和外泌体没有非常统一的鉴定标准,也有一些研究认为此种方法得到的是微泡不是外泌体。二是过滤离心,这种操作简单、省时,不影响外泌体的生物活性,但同样存在纯度不足的问题。三是密度梯度离心法,用此种方法分离到的外泌体纯度高,但是前期准备工作繁杂,耗时,量少。外泌体检测作为一种新型的液体活检热点技术已被许多临床科研机构普遍地应用于一些病症和疾病的无创诊断。
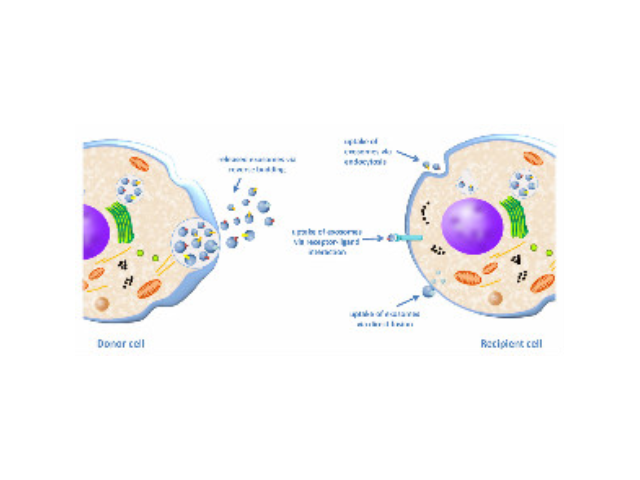
人体内多种细胞及体液均可分泌外泌体,包括内皮细胞、免疫细胞、血小板、平滑肌细胞等。当其由宿主细胞被分泌到受体细胞中时,外泌体可通过其携带的蛋白质、核酸、脂类等来调节受体细胞的生物学活性。外泌体介导的细胞间通讯主要通过以下三种方式:一是外泌体膜蛋白可以与靶细胞膜蛋白结合,进而靶细胞细胞内的信号通路。二是在细胞外基质中,外泌体膜蛋白可以被蛋白酶剪切,剪切的碎片可以作为配体与细胞膜上的受体结合,从而细胞内的信号通路。有报道称一些外泌体膜上蛋白在其来源细胞膜上未能检测出。使用PBS对膜进行洗脱即得到外泌体浓缩液。
人体内多种细胞及体液均可分泌外泌体,包括内皮细胞、免疫细胞、血小板、平滑肌细胞等。当其由宿主细胞被分泌到受体细胞中时,外泌体可通过其携带的蛋白质、核酸、脂类等来调节受体细胞的生物学活性。外泌体介导的细胞间通讯主要通过以下三种方式:一是外泌体膜蛋白可以与靶细胞膜蛋白结合,进而启动靶细胞细胞内的信号通路。二是在细胞外基质中,外泌体膜蛋白可以被蛋白酶剪切,剪切的碎片可以作为配体与细胞膜上的受体结合,从而启动细胞内的信号通路。有报道称一些外泌体膜上蛋白在其来源细胞膜上未能检测出。三是外泌体膜可以与靶细胞膜直接融合,非选择性的释放其所含的蛋白质、mRNA以及microRNA。外泌体携带大量特异性的蛋白质以及功能性的mRNAs、miRNAs等生物活性物质。宁波正规外泌体提取试剂销售厂家
外泌体的提取、分离方法:尺寸排阻色谱法和超滤法。杭州正规外泌体提取试剂
外泌体相关miRNA与肺病的诊断:miRNAs是一类含有20~25个核苷酸的非编码小RNA,能够通过下调或压制靶mRNAs来调节转录水平上的基因表达,目前非编码RNA被普遍发现存在于NSCLC患者外泌体中,参与一些病症的形成和演化过程。单个miRNA可能通过压制性复合物与多个mRNA结合,从而阻滞整个生物通路。因此,外泌体的miRNA具有成为NSCLC标志物的优势。Chen等在152例肺病患者的研究中初次报道了循环游离miRNA的表达,与75例健康者相比,发现了两种高表达的miRNA(miR-25和miR-223)。Rabinonowits等对27例肺病患者和9例健康人的血浆外泌体中12个miRNA的表达进行了评估,结果显示,12个一些病症相关的miRNA*在肺病患者中过度表达。Cazzoli等收集了30个血浆样本,发现4种外泌体miRNA(miR-378a、-379a、-139-5p、-200b-5p)在肺病患者血清中明显升高,用于筛查患者与健康人ROC曲线下面积(AUC)为0.908。离心除去细胞器,留取上清。杭州正规外泌体提取试剂
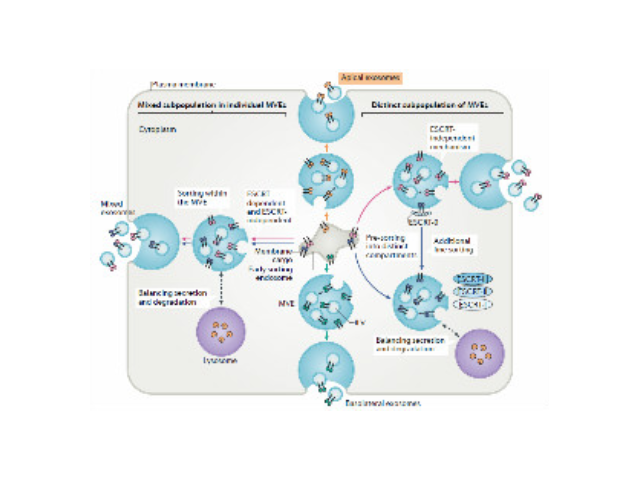
外泌体的形成与鉴定:首先,细胞膜内陷形成一个杯状结构,包括细胞表面蛋白和与细胞外环境相关的可溶性蛋白,导致早期胞内体(early-sortingendosome,ESE)的从头形成,或者是杯状结构直接和已经存在的ESEs融合;trans-高尔基体和内质网也能协助形成ESEs。ESE成熟后形成晚期胞内体(late-sortingendosomes,LSEs),较终形成MVBs(也称为多囊内小体)。MVBs是通过endosome限制膜向内凹(即质膜双凹)形成的,这一过程导致MVBs含有多个ILVs。MVB可以与溶酶体或自噬体融合,较终降解或与质膜融合释放作为外泌体的ILVs。外泌体表面蛋白包括四聚...
- 开封外泌体提取试剂供应商 2025-02-21
- 徐州外泌体提取试剂报价 2025-02-21
- 北京正规外泌体提取试剂厂家直销 2025-02-21
- 重庆外泌体提取试剂平均价格 2025-02-21
- 唐山正规外泌体提取试剂单价 2025-02-21
- 厦门正规外泌体提取试剂供应商 2025-02-21
- 杭州正规外泌体提取试剂 2025-02-20
- 外泌体提取试剂服务电话 2025-02-20
- 长沙正规外泌体提取试剂哪家便宜 2025-02-20
- 郑州外泌体提取试剂服务电话 2025-02-20
- 芜湖外泌体提取试剂价格 2025-02-19
- 成都正规外泌体提取试剂厂家现货 2025-02-19
- 南京外泌体提取试剂报价 2025-02-19
- 开封外泌体提取试剂哪里买 2025-02-19
- 杭州外泌体提取试剂哪家便宜 2025-02-19
- 厦门外泌体提取试剂服务电话 2025-02-19


- 开封外泌体提取试剂供应商 02-21
- 开封无血清细胞冻存液产品介绍 02-21
- 徐州外泌体提取试剂报价 02-21
- 宁波无血清细胞冻存液哪家好 02-21
- 厦门无血清细胞冻存液厂家供应 02-21
- 北京正规外泌体提取试剂厂家直销 02-21
- 杭州无血清细胞冻存液哪家便宜 02-21
- 苏州无血清细胞冻存液生产厂家 02-21
- 重庆外泌体提取试剂平均价格 02-21
- 唐山正规外泌体提取试剂单价 02-21