微量样本超多重检测的科研与临床价值:超多重检测芯片通过微流控分区技术,在单通道内集成21个**检测区(直径500微米),每个区域预埋特异性抗体,支持单次检测4-21个指标。以肺*筛查为例,芯片可一次性检测29种候选标志物(如CEA、CYFRA21-1、ProGRP),通过ROC曲线分析筛选出特异性>80%的组合(CEA+SA+CA242),诊断准确性从68%提升至92%。该芯片灵敏度达亚pg级(如IL-6检测下限0.5pg/mL),线性范围跨越3个数量级(1-1000pg/mL),且耗材成本较Luminex技术降低70%(单次检测成本<$50)。在科研领域,芯片支持微量样本(如穿刺活检液)中同时分析炎症因子(IL-1β、TNF-α)、血管生成标志物(VEGF)及代谢产物(乳酸),为**微环境研究提供多维度数据。临床验证显示,在100例乳腺*患者中,芯片检测的HER2与ER表达结果与IHC一致性达98%,为靶向***提供可靠依据。自动版数字 ELISA 芯片配套全自动加样仪与扫描仪,单个芯片支持≥8 样本同时反应,总时长 30 分钟。医疗检测数字ELISA高灵敏
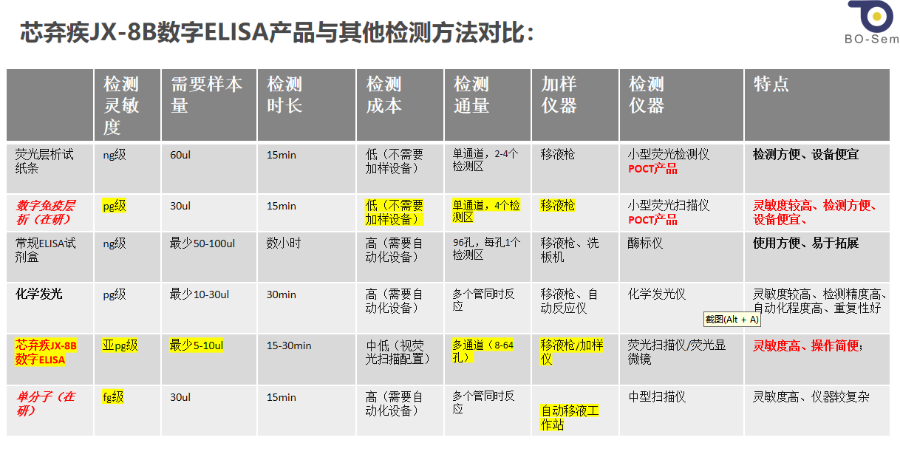
创新性的解决方案:芯弃疾JX-8B数字ELISA
我公司推出的数字化高灵敏ELISA芯片检测产品应用场景:适合生物实验室、医学实验室、科研市场、产品预研、产品开发、ELISA检测、动物病情检测等各种应用场景应用范围:各种高灵敏多重免疫检测,可替代各种ELISA试剂盒,及其他免疫检测产品。
将约5cm长的光纤束依次抛光使用30微米、9微米和1微米尺寸的金刚石研磨膜的机器。抛光光纤在0.025M盐酸溶液中化学蚀刻130秒,然后立即浸入水中以抑制反应。蚀刻后的光纤在水中复溶5秒,在水中洗涤5分钟,然后在真空下干燥。光纤束阵列的中心玻璃和包层玻璃的蚀刻速率差异caused4.5-μmdiameter孔在中心光纤中形成30。更初研究了不同蚀刻时间对孔深的影响。如果孔太深,则每个孔中沉积多个微珠。井口密封性被破坏;如果井口太浅,则无法将微球保留在井内,且观察到加载效率较差。对于单个微球而言,井口深度of3.25±0.5μm是比较好的,同时保持良好的密封性。 芯弃疾免疫检测数字ELISA灵活数字化高敏ELISA芯片,可以进行8孔、4孔的灵活检测。

多指标检测POCT芯片:急诊场景的即时检测先锋,多指标检测POCT芯片以卡片式紧凑设计与自动化操作,实现15-20分钟快速出结果,兼具高灵敏度与便捷性,成为院前急救、急诊场景的**工具。其沿用单分子捕获技术,灵敏度达pg/ml级别,可准确检测超敏肌钙蛋白T(hs-cTnT)、降钙素原(PCT)等关键指标,性能媲美化学发光法。配套小型化自动加样仪与扫描仪,无需复杂人工操作,***缩短急诊检测周期,为急性心梗、***性休克等危重症的快速诊断提供支持。在、流感病毒等传染性疾病筛查中,该芯片可快速鉴别抗原/核酸,助力**防控;在凝血功能、血气分析等项目中,即时反馈的检测结果为临床决策提供实时数据,推动POCT技术从单一指标检测向多指标联检升级,提升急诊救治效率与精细度。
抗体配对筛选的成本与效率优化,抗体筛选芯片通过高密度检测区设计与微量样本技术,大幅降低抗体开发的时间与物料成本。传统方法中,49种抗体配对需多次实验,耗时数天且消耗数百微升样本;而芯片技术*需1小时、5μl样本即可完成初步筛选,成本降低70%以上。其单通道多指标并行检测能力,支持不同反应条件(如pH、温度)的同步测试,快速筛选出比较好配对组合。在**标志物抗体开发中,该芯片可同时评估亲和力、特异性与交叉反应性,加速诊断试剂盒的研发进程,尤其适合初创企业与科研机构的高效筛选需求,推动抗体工程从试错性实验向精细化筛选转型。芯弃疾JX-8B数字ELISA,超敏检测,低可测试到亚皮克级;

芯弃疾JX-8B数字ELISA产品,为什么能做到?
芯弃疾JX-8B数字ELISA产品基本原理同somoa类似,
技术开创性领头产品:simoa单分子蛋白检测技术;
芯弃疾JX-8B数字ELISA产品参考simoa原理;Simoa®由现任于哈佛大学医学院的DavidWalt教授作为科学创始人于2007年创立。DavidWalt是美国的工程院,艺术院和医学院三院院士。2010年,DavidWalt将Simoa®技术以封面文章的形式发表在《NatureBiotechnology》上,此技术开始为大众所知并引起业界轰动。 芯弃疾单分子ELISA检测试剂盒,多重超敏检测,多重指标也能检测到亚皮克级!单分子级别数字ELISA芯片
芯弃疾JX-8B数字ELISA,超敏检测,理论可达飞克级;医疗检测数字ELISA高灵敏
单分子芯片技术原理与超敏检测能力:芯弃疾单分子芯片基于数字ELISA技术,采用微米级捕获结构与二次流原理,通过微流控设计在单个芯片上形成数十万至百万个**反应单元。每个反应单元由表面功能化的磁珠构成,磁珠直径约5微米,通过微孔阵列与流体动力学优化实现高密度、高稳定性固定(捕获效率>95%)。检测过程中,靶标分子与磁珠表面抗体结合后,采用量子点标记的二抗进行信号放大,通过高分辨率荧光显微镜(如20×物镜)对每个磁珠的荧光强度进行成像分析。其**突破在于单分子级信号分辨能力,例如IL-6检测限低至0.2pg/mL(传统ELISA为1-5pg/mL),灵敏度提升5-25倍。该技术通过全流程芯片集成(样本裂解、反应孵育、信号读取),将试剂消耗量减少至传统方法的1/10(*需5μL血清),并支持微量样本(如10μL房水或泪液)中检测神经退行性疾病标志物(如NfL浓度低至0.5pg/mL)。临床研究表明,该芯片可在阿尔茨海默症临床症状出现前16年检测到Aβ42异常聚集,为早期干预提供关键时间窗口。此外,芯片兼容自动化操作系统,单次检测时间缩短至2小时,较传统数字ELISA效率提升3倍。医疗检测数字ELISA高灵敏