- 品牌
- 上海司鼎生物科技有限公司
- 型号
- 型号齐全
制作组织芯片,首先要收集和整理供体组织样本,确保样本的质量和代表性。对样本进行固定、包埋等预处理后,使用组织阵列仪从供体蜡块中采集组织芯。在采集过程中,需精确控制组织芯的大小和位置。将采集好的组织芯按照预定的阵列模式移植到受体蜡块中,制成组织芯片蜡块。随后,对蜡块进行切片,将切片裱贴在载玻片上。在进行实验检测前,还需对切片进行脱蜡、水化等处理。根据实验目的,选择合适的检测方法,如免疫组化、原位杂交等,然后对实验结果进行观察和分析。原位杂交解决方案适用于多种类型样本,在基础科研与临床研究中展现出强大的兼容性。杭州多重免疫荧光服务
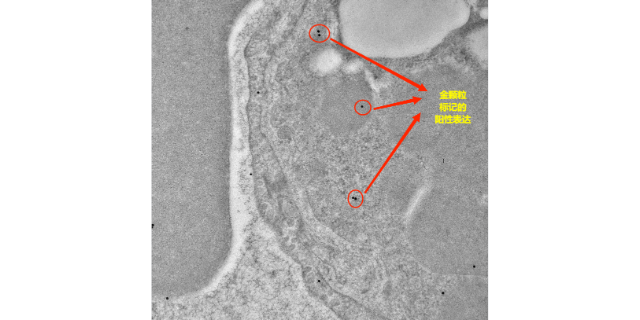
在病理学研究中,组织芯片发挥着重要作用。对于瘤子病理诊断,它能够快速对大量瘤子样本进行多种标志物的检测,辅助确定瘤子的类型、分级和分期。例如,通过检测肺病组织芯片中特定基因突变相关蛋白的表达情况,帮助区分肺腺病和鳞病,并进一步判断其恶性程度。在疾病的病理机制研究方面,组织芯片可用于分析不同疾病状态下组织中基因表达、蛋白质表达和细胞形态变化的相关性。比如在神经退行性疾病研究中,利用组织芯片观察不同脑区神经元的病理改变以及相关蛋白的异常聚集情况,探索疾病的发病机制。同时,组织芯片也有助于病理诊断的标准化和质量控制,通过对大量已知病例的组织芯片检测,建立诊断标志物的表达标准,提高病理诊断的准确性和一致性。温州组织芯片免疫组化平台组织芯片免疫荧光方案在疾病研究和医治靶点验证方面具有重要用途。
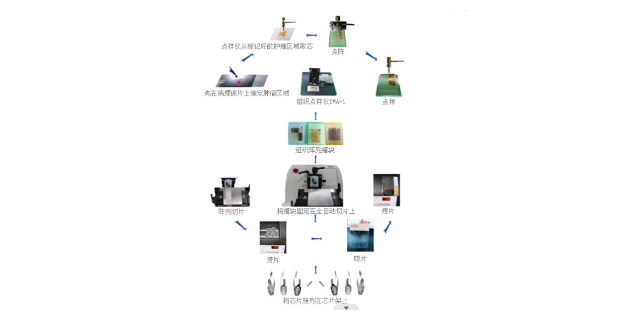
组织芯片免疫荧光方案的重点功能在于其高通量检测能力和数据整合能力。通过将多个组织样本排列在一张载玻片上,该方案能够在有限的空间内实现对多个组织的同时分析。这种高通量检测不仅提高了实验效率,还减少了样本之间的差异,降低了实验误差。此外,组织芯片免疫荧光方案能够将不同靶标的检测结果整合在同一张切片上,便于研究人员进行统一分析和比较。这种数据整合能力使得研究人员能够更直观地观察不同靶标之间的相互关系,为深入理解疾病机制和开发医治策略提供了重要依据。
原位杂交技术服务遵循严格的标准化实验流程,确保检测结果的可靠性与可重复性。实验起始于样本制备,根据样本类型选择适宜的处理方式,如石蜡切片需依次完成脱蜡、水化及抗原修复,细胞样本则需进行固定和透化处理,以保证探针顺利进入样本与靶核酸结合。探针设计与标记是实验关键环节,需依据目标核酸序列特征定制特异性探针,并选择合适标记方法。杂交过程中,精确控制杂交温度、时间及杂交液组成,保证探针与靶核酸充分结合。杂交后通过严谨的洗涤步骤去除未结合探针,减少背景信号干扰。继而利用相应检测系统对杂交信号进行可视化呈现,每个步骤均严格把控,确保实验质量稳定。原位杂交技术服务以核酸碱基互补配对原则为基石,实现特定核酸序列在细胞或组织原位的可视化检测。
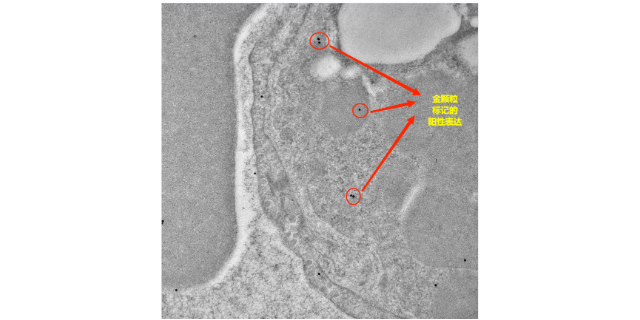
质量把控是组织芯片免疫组化服务的生命线,贯穿于整个服务流程的始终。在实验准备阶段,对实验试剂进行严格筛选,从抗体、显色剂到各种缓冲液,都需经过多轮质量检测,确保其纯度、活性和特异性符合实验要求。仪器设备的定期校准和维护同样不可或缺,高精度的切片机、显微镜、扫描仪等设备只有在性能稳定的状态下,才能保证实验操作的精确性和数据采集的准确性。实验人员作为操作主体,必须接受系统的专业培训,熟练掌握实验流程和操作技巧,同时具备严谨的科学态度和质量意识。在实验过程中,严格设置阳性和阴性对照样本,阳性对照用于验证实验体系的有效性,阴性对照则用于排除非特异性染色的干扰。实验结束后,对原始数据进行多次审核和验证,通过重复实验和交叉验证等方式,进一步确认结果的可靠性,确保每一份检测报告都能真实、准确地反映样本的实际情况。多种位点组织芯片应用对样本类型具有广阔的兼容性。合肥组织芯片免疫荧光方案
组织芯片免疫荧光方案的重点功能在于其高通量检测能力和数据整合能力。杭州多重免疫荧光服务
组织芯片免疫组化定制在生物医学研究和临床诊断中具有广阔的应用范围,涵盖了从基础研究到临床实践的多个领域。在基础研究中,该技术可用于细胞生物学、肿块学、免疫学、神经科学等多个学科。例如,在肿块研究中,组织芯片免疫组化定制能够同时检测肿块细胞和免疫细胞的多种标志物,揭示肿块微环境的免疫状态和细胞间相互作用,帮助研究人员深入理解肿块的发生、发展机制以及免疫逃逸过程。在神经科学研究中,该技术可用于检测神经元、胶质细胞和突触的多种标志物,为神经退行性疾病的研究提供重要支持。在临床诊断方面,组织芯片免疫组化定制可用于检测多种生物标志物,辅助疾病的早期诊断、预后评估以及医治效果的监测。例如,在肿块诊断中,该技术能够同时检测肿块标志物和免疫细胞标志物,为个性化医治方案的制定提供依据。此外,组织芯片免疫组化定制还可用于药物开发中的靶点筛选和疗效评估,通过检测药物靶点和细胞应答标志物,直观地评估药物的作用效果。杭州多重免疫荧光服务
多重免疫荧光平台凭借其独特的酪胺信号放大(TSA)技术,展现出明显的多重检测与高灵敏度优势。TSA技术利用辣根过氧化物酶(HRP)催化酪胺自由基与组织抗原周围的酪氨酸残基发生共价结合,从而在抗原位点上沉积大量荧光信号。这一过程不仅明显增强了信号强度,还使得该平台能够检测到低丰度的靶标,这对于研究复杂的生物过程和组织微环境至关重要。与传统的免疫组化技术相比,多重免疫荧光平台能够有效避免荧光信号的串色问题,确保检测结果的准确性和可靠性。此外,该平台兼容多种抗体和荧光染料,可在同一组织切片上进行多轮染色,有效提高了实验效率和数据丰富度。这种多重检测能力使得研究人员能够在同一张切片上同时观察多个标志物...
- 淮南多重免疫荧光哪家靠谱 2025-06-28
- 佛山组织芯片免疫组化哪家专业 2025-06-27
- 杭州多重免疫荧光服务 2025-06-27
- 湖州组织芯片免疫荧光定制 2025-06-27
- 温州多重免疫荧光技术服务 2025-06-27
- 佛山多种位点组织芯片用途 2025-06-27
- 湖州原位杂交技术 2025-06-26
- 湖州原位杂交方案 2025-06-26
- 无锡原位杂交定制 2025-06-25
- 深圳原位杂交哪家靠谱 2025-06-25
- 深圳多种位点组织芯片哪家靠谱 2025-06-22
- 厦门多种位点组织芯片解决方案 2025-06-21
- 珠海多种位点组织芯片哪家好 2025-06-21
- 漳州组织芯片免疫荧光应用 2025-06-20
- 芜湖多种位点组织芯片平台 2025-06-20
- 佛山多重免疫荧光哪家靠谱 2025-06-19


- 温州多重免疫荧光技术服务 06-27
- 佛山多种位点组织芯片用途 06-27
- 湖州原位杂交技术 06-26
- 绍兴化学膜片钳技术特点 06-26
- 广州光遗传技术服务 06-26
- 嘉兴化学遗传技术哪家靠谱 06-26
- 湖州原位杂交方案 06-26
- 无锡原位杂交定制 06-25
- 光遗传膜片钳技术方案 06-25
- 深圳原位杂交哪家靠谱 06-25